“Quando você fala para alguém que está com câncer, as pessoas começam a te velar, praticamente te enterram com frases e olhares”, desabafa o oncoinfluencer Heitor William, 28 anos, que recebeu o diagnóstico de LPA (leucemia promielocítica aguda) em 2020, no início da pandemia de Covid-19. Trata-se de um subtipo da doença que ocorre quando a medula óssea não é capaz de produzir células sanguíneas saudáveis o suficiente.
Apesar de comum, esse tipo de reação é fruto da desinformação e de uma cultura que ainda trata o câncer como um tabu, algo indesejável e sobre o qual é difícil de falar.
O aposentado Eduardo Picirillo visita o hospital A.C. Camargo, onde fez tratamento
Edu Garcia/R7 - 26.04.2023Em meio às incertezas geradas pelo novo vírus, além de ter de lidar com a descoberta do câncer, um subtipo de LMA (leucemia mieloide aguda), William decidiu enfrentar o estigma social da doença: passou a compartilhar seu tratamento nas redes sociais e mostrou as dificuldades que um paciente oncológico enfrenta de maneira leve e informativa. Ele tem 24 mil seguidores no Instagram.
Na época em que recebeu seu diagnóstico, o influenciador chegou a ouvir de um médico que tinha apenas quatro dias de vida, dado o avanço da doença — ele tinha 96% de seu corpo tomado.
Hoje, o influenciador é prova de que o câncer já não é mais uma sentença de morte — os últimos exames mostraram taxas de recuo de 99,6% da doença. E, apesar de a remissão estar quase completa, ele continua em tratamento com quimioterapia intramuscular, por meio de injeções (diferentes da quimio tradicional, que é endovenosa), e que estão programadas até julho. Depois, passará para a quimioterapia via oral.
Segundo Eduardo Rego, coordenador do serviço de leucemia aguda do Icesp (Instituto do Câncer do Estado de São Paulo), onde William faz o tratamento, a LMA é considerada um diagnóstico raro, com de 2,5 a 5 casos para cada 100 mil habitantes.
Por mais que a mortalidade da doença ainda seja alta, os avanços no diagnóstico e no tratamento mostram que é cada vez maior a chance de os pacientes terem um prognóstico positivo.
“Embora não seja uma sentença de morte, nós temos que ver que o câncer vai se tornar a principal causa de mortalidade no mundo. Isso não quer dizer que todo mundo que tem câncer vai morrer. Diferentemente do que a gente tinha antes, 20 anos atrás, em que a maioria dos pacientes diagnosticados viria a morrer, hoje nós podemos dizer que curamos mais de 60% dos cânceres diagnosticados”, afirma Roberto Gil, oncologista e presidente do Inca (Instituto Nacional do Câncer).

Eduardo Picirillo visita o hospital A.C. Camargo, onde fez seu tratamento para o câncer
Edu GarciaDe acordo com o Inca, foram confirmados 1.556.824 óbitos relacionados à doença em 2020. No entanto, as altas taxas não necessariamente significam um avanço do câncer no Brasil.
Se compararmos os últimos dados de mortalidade fornecidos pelo instituto com os de 20 anos atrás (1.002.340 mortes em 2003), observamos uma alta no número de diagnósticos e de mortes. Roberto Gil explica que isso se deve aos avanços na detecção precoce da doença, somados ao aumento e ao envelhecimento da população.
Ele afirma que, no Brasil, houve uma inversão da pirâmide populacional, com maior número de idosos em relação a jovens, o que aumentou a incidência da doença. Isso porque o câncer, em 90% dos casos, acontece por um acúmulo de mutações celulares que ocorrem ao longo da vida, com aparecimento, geralmente, a partir dos 50 anos. Já os outros 10% seriam de origem hereditária.
Demais fatores, como o aumento das taxas de sedentarismo, a piora na qualidade da alimentação e a maior concentração urbana (com locais cada vez mais submetidos a processos de desenvolvimento de substâncias cancerígenas) também fizeram com que houvesse um aumento na incidência de tumores.
Entre os cânceres que ainda têm altos números de letalidade estão os de traqueia, brônquios e pulmão. Só em 2020, foram registrados 28.620 óbitos relacionados a esses tipos.

Mas os pacientes podem ir na contramão das estatísticas e conseguir se recuperar.
Foi o que aconteceu com Eduardo Picirillo, 65 anos. Em 2018, após voltar de uma viagem, ele percebeu que estava com dificuldades relacionadas à percepção de espaço. Em uma primeira consulta, ouviu que se tratava de uma sinusite.
Na mesma semana, os sintomas se repetiram. Ele foi submetido a uma tomografia para uma investigação mais completa, e os médicos encontraram um tumor cerebral. Com o diagnóstico recebido na noite de uma quinta-feira, a cirurgia para a retirada das células cancerígenas foi marcada para domingo.
O material foi encaminhado para biópsia, que revelou algo inesperado: o tumor no cérebro era a metástase de um câncer originado no pulmão.
O tratamento de Picirillo consistiu, além da cirurgia para retirar o tumor cerebral, na realização de radioterapia, seguida pela combinação de quimio com imunoterapia. Devido à reincidência de pequenos tumores cerebrais, que não poderiam ser operados, ele teve ainda que passar por novas sessões do primeiro tratamento.
O aposentado se encontra em remissão e sem sinais da doença desde 2021. Faz apenas os exames de acompanhamento — PET Scan anual, ressonância magnética da cabeça a cada seis meses, tomografia e exames de sangue a cada três meses — para verificar se há algum sinal de tumores.

Eduardo Picirillo toca o sino, símbolo do fim do tratamento de câncer, no hospital A.C. Camargo
Edu GarciaPicirillo, como ex-paciente, entende que a grande chave para sua remissão vem dos avanços nos tratamentos. Mas nem todo mundo consegue ter acesso aos mesmos recursos a que ele teve.
O seu câncer foi tratado em um dos centros de excelência oncológica do país, o hospital A.C. Camargo, em São Paulo, e, mesmo assim, quando recebeu a indicação para a imunoterapia (método que induz as próprias células imunes do corpo a lutar contra a doença), houve um impasse. Apesar de esse procedimento já ser aprovado pela Anvisa (Agência Nacional de Vigilância Sanitária), naquele momento ele ainda não era coberto pelos convênios.
Na época, cada sessão, segundo seu relato, custava cerca de R$ 70 mil. Ele recorreu à ajuda de advogados para poder realizar o tratamento. Foram necessários apenas dois dias após ele obter uma medida liminar para que o plano de saúde cedesse e incorporasse a imunoterapia aos tratamentos custeados pela operadora.
No entanto, a imunoterapia, um dos tratamentos mais modernos oferecidos, até hoje só está disponível em hospitais particulares e nos centros de excelência. O SUS (Sistema Único de Saúde) oferece a imunoterapia para poucos diagnósticos e em poucas unidades, devido ao seu alto custo.
Carlos Gil, diretor médico do grupo Oncoclínicas e presidente da SBOC (Sociedade Brasileira de Oncologia Clínica), explica que, pelo SUS, esse tratamento está disponível apenas para melanomas (cânceres de pele considerados os mais agressivos de seu tipo) e, mesmo com a sua aprovação pelo Ministério da Saúde, ainda há falta de recursos para oferecê-lo.
“Existe uma distância do que pode ser oferecido pela saúde suplementar [planos de saúde] e o que pode ser oferecido pelo SUS. Essa desigualdade, para alguns tipos de tumor, é o equivalente a uma diferença de dez anos em termos de tecnologia. Provavelmente, essa discrepância é o grande desafio da oncologia nacional”, avalia.
De acordo com o médico, hoje o SUS oferece como tratamentos as cirurgias para retirada de tumores, a quimioterapia, a radioterapia e algumas opções limitadas de drogas-alvo, direcionadas a cada tipo de tumor.
Porém, a própria radioterapia é uma técnica a que poucos pacientes têm acesso pelo sistema público. Dados da SBRT (Sociedade Brasileira de Radioterapia) informam que, anualmente, cerca de 73 mil pacientes não conseguem receber esse tratamento.
Além disso, ele afirma que a maior concentração de procedimentos está no Sul e no Sudeste, com poucos aparelhos distribuídos nas demais regiões.
A verificação da SBRT revela que apenas 120 municípios em todo o Brasil contam com o tratamento via SUS. O país possui um total de 263 máquinas que prestam serviço radioterápico, das quais 140 estão na região Sudeste; em segundo lugar, a região com mais equipamentos é a Sul, com 51 máquinas.
Já as regiões Nordeste, Centro-Oeste e Norte possuem, respectivamente, 37, 20 e 15 aparelhos.
Se em relação ao acesso às tecnologias existe uma defasagem, o mesmo não pode ser afirmado sobre os medicamentos antineoplásicos (os remédios usados no tratamento do câncer) e os atenuantes de efeitos do tratamento, que têm grande quantidade aprovada no Brasil.
Em levantamento realizado pelo R7, por meio da Lei de Acesso à Informação, entre 2003 e 2022 a Anvisa aprovou 449 medicamentos dessa classe. O ano com maior número de aprovações foi 2018, com 83 drogas, seguido por 2022 (com 56 aprovações) e 2019 (49 aprovações).
Os dados podem ser divididos em dois grupos, de acordo com a cronologia e o intervalo de tempo: de 2003 a 2015 e de 2016 a 2022.
Nota-se que o segundo grupo evidencia os avanços nos tratamentos nos últimos anos, quando, em 2016, foram concedidas 24 liberações medicamentosas pela agência. Desde então, as aprovações dos remédios não são menores do que 20 ao ano.
Já quando observado o período de 2003 a 2015, o máximo de concessões foi de 16 medicamentos, no ano-limite. O pior índice foi em 2004, com apenas três tratamentos liberados.

Entre os avanços do grupo mais recente, está a aprovação do trióxido de arsênio, em 2017. A droga, segundo o coordenador do Icesp, assim como um dos tratamentos utilizados por William — o ácido all-trans retinoico, conhecido como ATRA —, é de uma classe de medicamentos que não são quimioterápicos, o que mostra a inovação nos fármacos.
As últimas décadas foram marcadas pelas transformações no diagnóstico. Rego afirma que a principal mudança foi na percepção da doença, tanto por profissionais como por pacientes, com uma menor estigmatização.
“Hoje nós entendemos que o câncer é potencialmente curável em muitos casos. Que muitas vezes ele ocorre por essas alterações genéticas não hereditárias e que o diagnóstico precoce auxilia muito no melhor prognóstico do tratamento”, elucida o oncologista do Icesp.
Rodrigo Munhoz, oncologista do Hospital Sírio-Libanês, em São Paulo, reforça que as esperanças aumentaram devido ao maior controle de fatores de risco e ao diagnóstico precoce a partir do rastreamento, como é o caso dos cânceres de mama e de testículo.
Ele diz que o melhor entendimento do câncer, aliado a uma classificação dos tumores mais adequada, trouxe uma compreensão mais correta dos fatores de risco, do comportamento celular e dos tratamentos.
“É uma descoberta contínua. Estamos entendendo o que contribui e de qual forma no desenvolvimento de cada câncer. Naturalmente, isso auxilia na elaboração de estratégias de prevenção”, afirma Munhoz.
A evolução dos tratamentos contribuiu para as taxas de sucesso das recuperações. Como exemplo, Rego usa o diagnóstico de William.
“A LPA é uma doença que teve seu prognóstico mais drasticamente alterado para melhor. Antes dos anos 2000, antes da introdução desse medicamento Atra, parte dos pacientes acabava morrendo de complicações hemorrágicas da doença. A gente perdia muitos pacientes nas duas primeiras semanas após o diagnóstico”, explica.
E continua: “A melhor identificação das bases genéticas e dos agentes [medicamentosos] permitiu que fizéssemos um tratamento mais direcionado, mais precoce e com uma duração de resposta muito mais longa. Então a gente pode falar em cura desses pacientes com muito mais certeza do que 20, 25 anos atrás”.
Munhoz lembra que houve melhora e evolução no diagnóstico e completa: a tendência é um aprimoramento cada vez maior.
“Daqui a alguns anos, podemos ter exames mais sensíveis, como a utilização de testes sanguíneos para o diagnóstico de câncer dentro do conceito de DNA circulante, uma técnica menos invasiva do que os exames atuais para rastreamento, como o PET-Scan. Ainda não é uma realidade, mas daqui algumas décadas pode ser”, reitera o oncologista do Sírio-Libanês.
Uma técnica parecida está em pesquisa para o diagnóstico e outra já está aprovada para o direcionamento do tratamento. Ambas fazem parte das chamadas “biópsias líquidas” e diferem pelo meio de detecção: por CTCs (células tumorais circulantes) ou por DNA, respectivamente.
Andrea Motoyama, coordenadora do Laboratório de Patologia Molecular do Câncer da Faculdade de Medicina da UnB (Universidade de Brasília), explica que, para ambos os casos, são coletados de 4 ml a 5 ml de sangue do paciente. A amostra é enviada para a análise genética em laboratório, onde são utilizadas máquinas, os NGS (Sequenciadores de Nova Geração), que detectarão a presença dos genes cancerígenos.
Após a análise da máquina, um profissional — geralmente um patologista — dá seu parecer.
O rastreamento biológico molecular para diagnóstico é feito a partir da análise das CTCs e, no Brasil, está apenas em campo de pesquisa, ainda sem a liberação da Anvisa para a sua aplicação.
Já o rastreamento biológico molecular por DNA teve sua autorização concedida. Nesse caso, a tecnologia não faz o diagnóstico, mas analisa a genética do câncer e do paciente para estabelecer a melhor abordagem terapêutica, com maior eficiência.
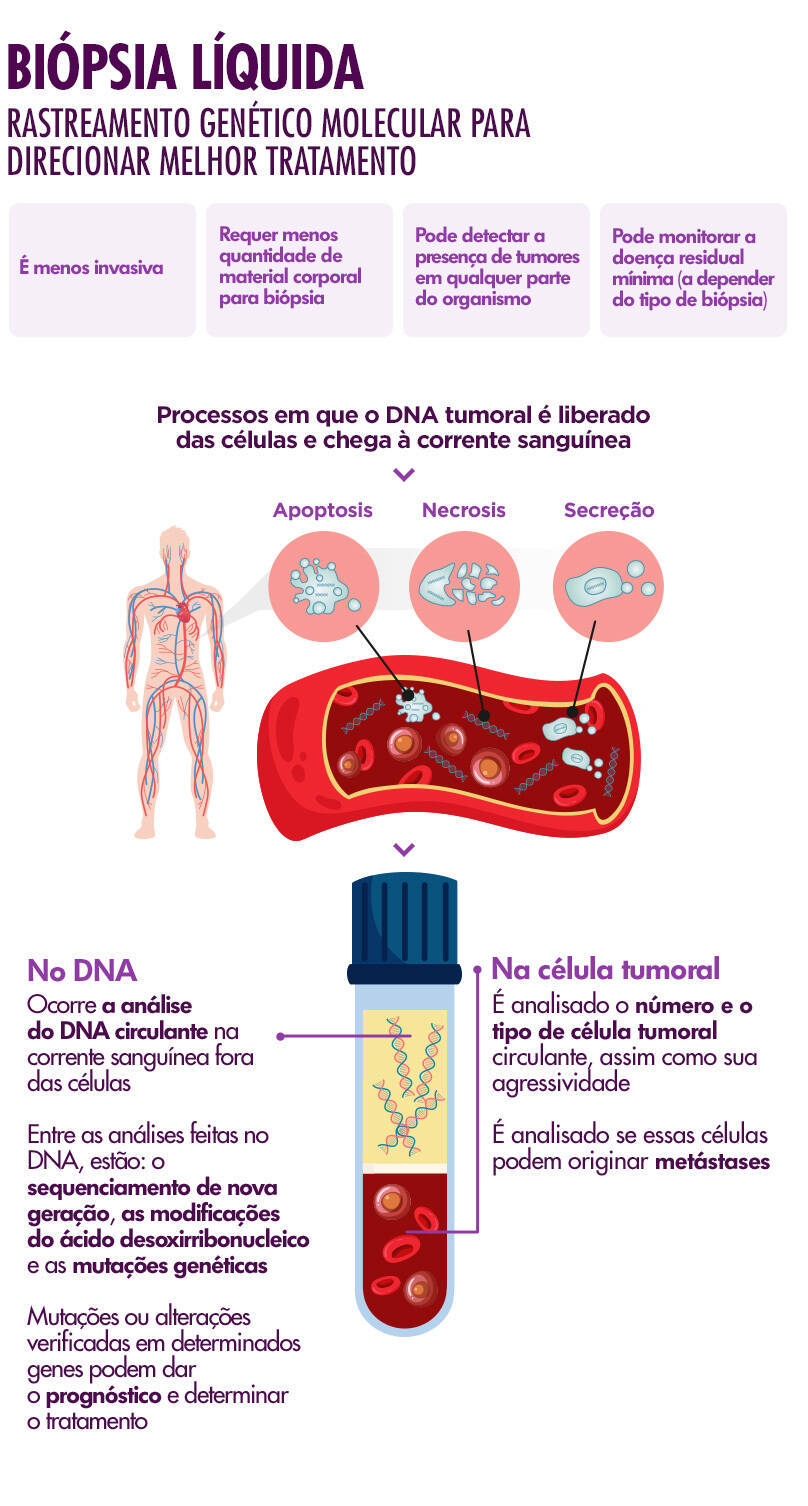
Andrea classifica a técnica como a grande chave para diagnóstico, acompanhamento e tratamento do câncer para os próximos anos.
“Precisamos que a biologia molecular nos ensine como é o desenvolvimento dessa doença. A pesquisa tem que desenvolver, cada vez mais, biomarcadores, ou seja, marcadores moleculares que nos digam quando essa medicação pode ser mais efetiva, para que haja uma seleção. Assim, em vez de usar a mesma droga para todos, eu indico conforme a resposta que o tipo de câncer terá. Isso vai permitir a individualização de cada tratamento a partir da individualização de cada câncer. A efetividade aumenta e o sucesso terapêutico, também. Então, consigo poupar, porque podemos priorizar os recursos da melhor maneira ”, finaliza o presidente do Inca.
Reportagem: Giovanna Borielo
Edição: Vivian Masutti
Fotos: Edu Garcia
Arte R7: Matheus Vigliar, Omar Sabbag e Sabrina Cessarovice
Gerente de Produção Audiovisual: Douglas Tadeu
Produção Audiovisual: Julia de Caroli e Matheus Mendes
Op. Captação Audiovisual: Mariana Lima
Edição: Ed Sabatine e Roberta Azevedo
Coord. Video e Prod. Conteúdo: Danilo Ferreira Barboza
Designer Gráfico Audiovisual: Marisa Kinoshita
In memoriam: Nelson Ferreira e todos os outros pacientes vítimas de câncer